指針等が様々あって 30 40 年前の状況とは全然違う現状できっちりとした crb ではなくても irb での審査とか同意説明文書の文書にとるとか副作用報告についても倫理指針にも詳細な規定があるでしょうし臨床研究法の対象から外れるからといってとんでもなく質の悪い臨床試験. 学外の方はこちら crb佐賀大学臨床研究審査委員会 特定臨床研究の開始時手続きに関するチェックリスト厚労省hp掲載につきましてはこちらをご参照ください 1事前相談 臨床研究相談申込書ダウンロード学内限定.
Bv Clinical Crb 臨床研究法対応版 株式会社ビッグバン
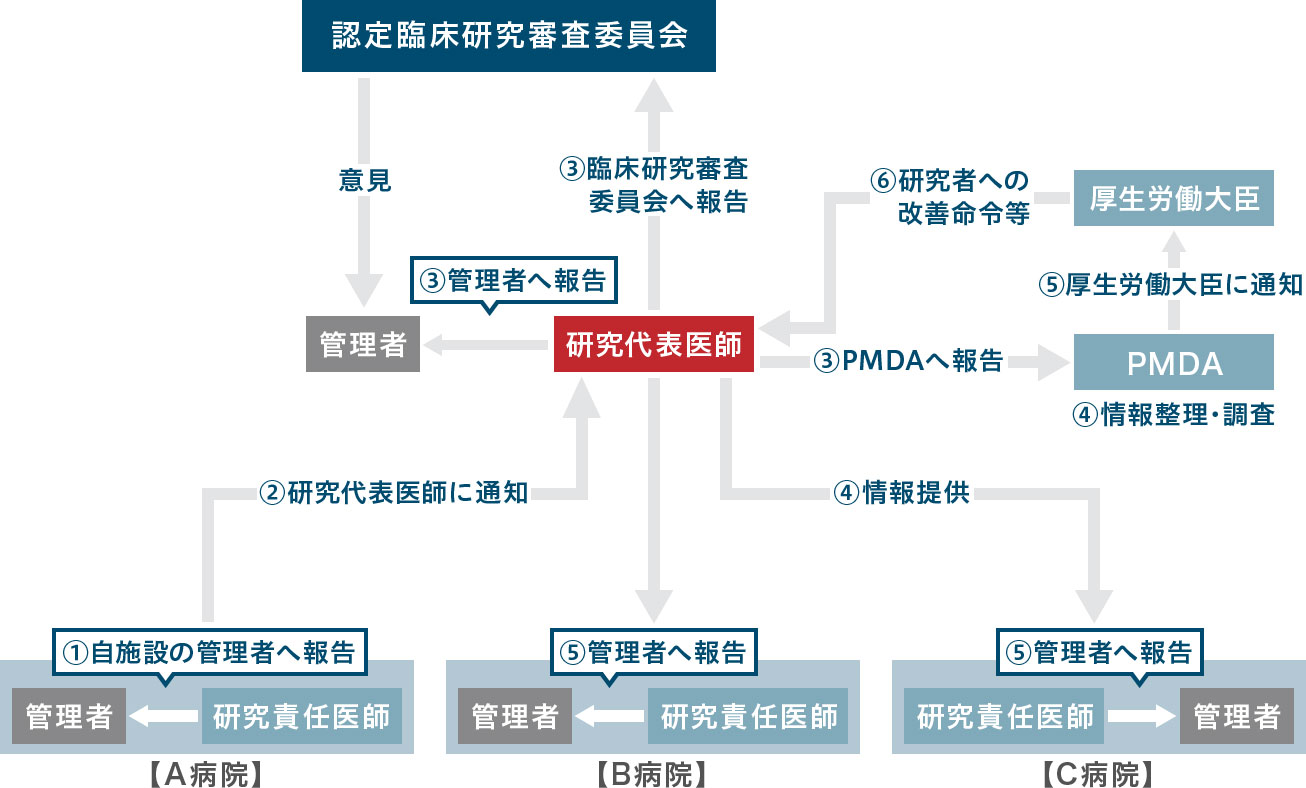
疾病 不具合報告 神戸大学臨床研究審査委員会
臨床研究法
性のSecondary Sponsor とは共同研究における企業を指すの か 回答案 共同研究において企業が研究資金の拠出以外に研究計画立 案に関与していた場合は当該企業はSecondary Sponsor に該 当する 臨床研究治験活性化協議会平成30年度第.

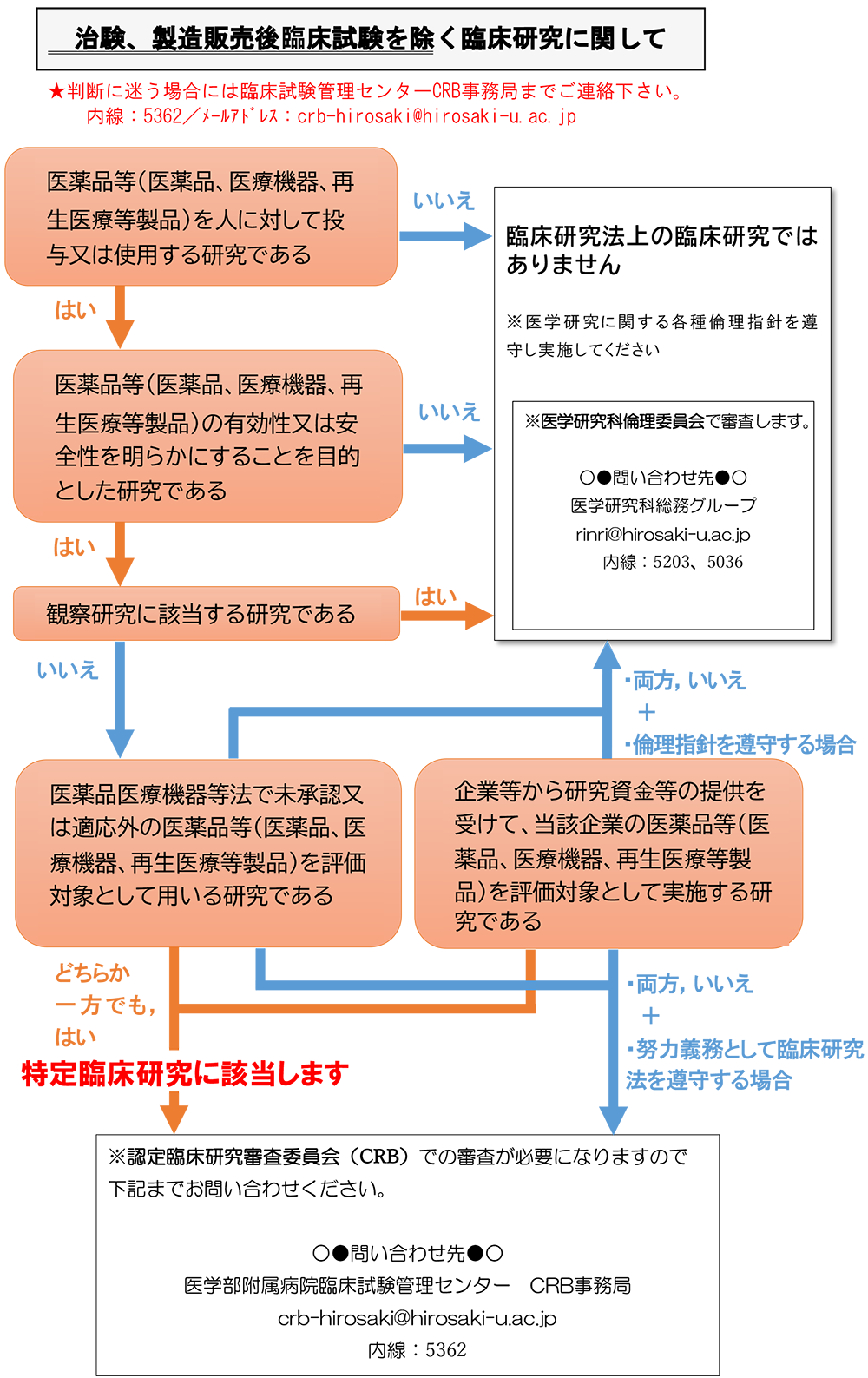
Crb とは 臨床 研究. Npo skin セミナーのとは. 臨床研究とは 医薬品や医療機器に関して人での有効性や安全性を調べる医学研究のことです 病気の予防診断治療方法の改善や病気の原因の解明患者さんの生活の質の向上を目的とし. 立案中の研究が臨床研究法で定められる特定臨床研究に該当するかどうか下記のフローチャートでご確認いただけます 臨床研究とは臨床研究法第2条1項において医薬品等を人に対して用いることにより1 当該医薬品等の有効性又は安全性を明らかにする2研究であると定義さ.
臨床研究法において臨床研究とは 医薬品等を人に対して用いることにより当該医薬品等の有効性又は 安全性を明らかにする研究 と定められています. 210927 第313回治験審査委員会議事録概要を公開しました 210803 第312回治験審査委員会議事録概要を公開しました. 211015 第122回医薬品等臨床研究倫理審査委員会議事録概要を公開しました 第314回治験審査委員会議事録概要を公開しました new.
研究責任医師は臨床研究法の下の特定臨床研究及び臨床研究以下臨床研究とするについて省令または研究計画書に不適合1 であると知ったときは実施医療機関の管理者に報告することが義務付けられています 不適合のうち特に重大な不適合2 事案が判明した場合は. 東京大学臨床研究審査委員会が2018年5月16日付で臨床研究法に伴う認定臨床研究審査委員会として認定 されました認定番号 CRB3180024 東京大学の学内ルールに則り2018年4月1日の当該法施行後に学内規程を制定しました関係でこのタイミン.
本委員会について 臨床試験管理センター 弘前大学医学部附属病院
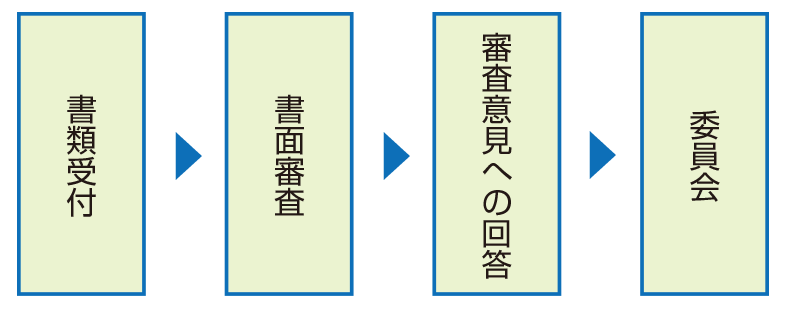
臨床研究法に基づく臨床研究審査委員会 Crb 国立がん研究センター 東病院
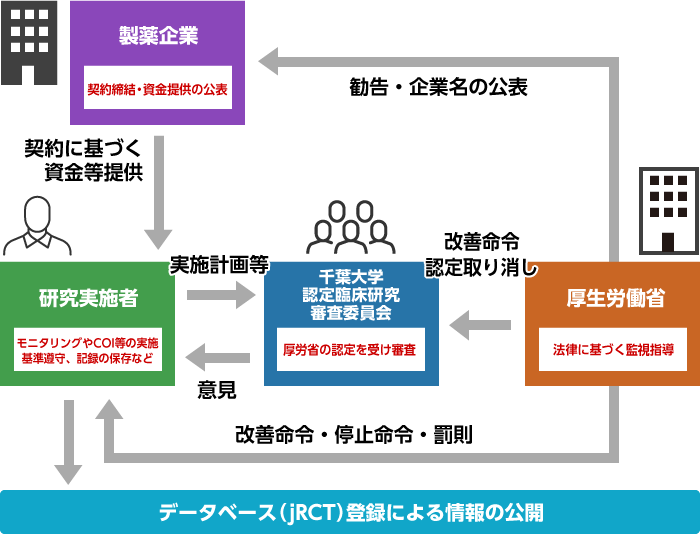
認定臨床研究審査委員会について 厚生労働大臣認定 千葉大学 臨床研究審査委員会

総合臨床研究センター

特定臨床研究に関する業務手順書 東邦大学医療センター大森病院 治験 臨床研究管理部
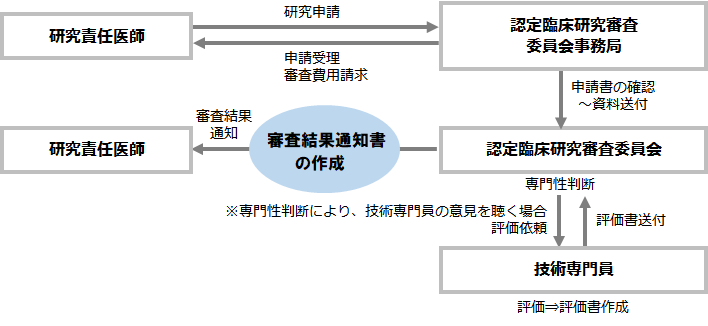
特定臨床研究実施の流れ 学外の方 佐賀大学医学部附属病院臨床研究センター

臨床研究法に基づく中央病院臨床研究審査委員会について 国立がん研究センター 中央病院
2
